- Συγγραφέας Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:36.
- Τελευταία τροποποίηση 2025-06-01 07:36.
Η βασική διαφορά μεταξύ του μονοξειδίου του αζώτου και του πεντοξειδίου του αζώτου είναι ότι το μονοξείδιο του αζώτου είναι ένα άχρωμο αέριο ενώ το πεντοξείδιο του αζώτου είναι ένα λευκό στερεό.
Το μονοξείδιο του αζώτου και το πεντοξείδιο του διαζώτου είναι χημικές ενώσεις που περιέχουν άζωτο και οξυγόνο. Αυτά είναι οξείδια του αζώτου. Ωστόσο, έχουν διαφορετικές χημικές και φυσικές ιδιότητες.
Τι είναι το μονοξείδιο του αζώτου;
Το μονοξείδιο του αζώτου είναι μια ανόργανη ένωση με τον χημικό τύπο ΝΟ. Το ονομάζουμε μονοξείδιο του αζώτου αφού είναι οξείδιο του αζώτου. Στην πραγματικότητα είναι μια ελεύθερη ρίζα επειδή έχει ένα ασύζευκτο ηλεκτρόνιο. Επιπλέον, είναι ένα ετεροπυρηνικό διατομικό μόριο.
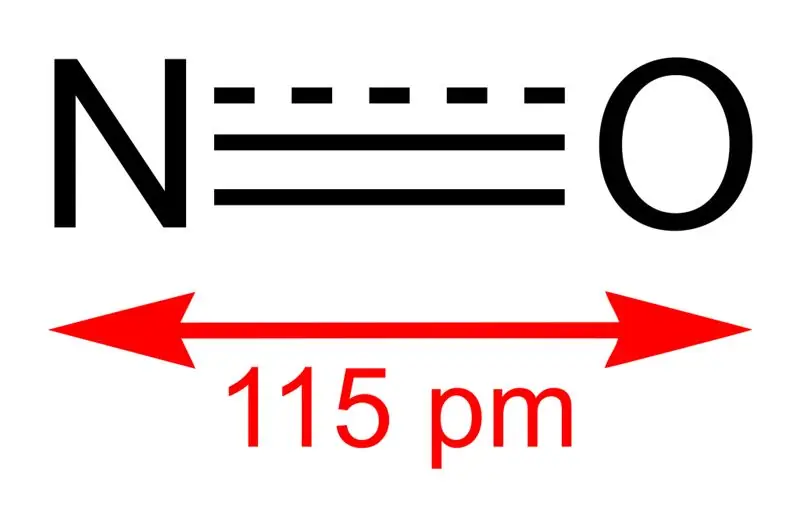
Εικόνα 01: Δομή του μονοξειδίου του αζώτου και το μήκος δεσμού μεταξύ N και O
Η μοριακή μάζα αυτής της ένωσης είναι 30 g/mol. Εμφανίζεται ως άχρωμο αέριο. Επιπλέον, το σημείο τήξης του είναι −164 °C ενώ το σημείο βρασμού είναι −152 °C, που είναι πολύ μικρές τιμές σε σύγκριση με εκείνες άλλων οξειδίων του αζώτου. Μπορούμε να παράγουμε αυτήν την ελεύθερη ρίζα μέσω οξείδωσης της αμμωνίας στους 850 °C παρουσία καταλύτη πλατίνας. Ωστόσο, σε εργαστηριακή κλίμακα, μπορούμε να το παρασκευάσουμε με την αναγωγή του αραιού νιτρικού οξέος με χαλκό.
Τι είναι το Dinitrogen Pentoxide;
Το πεντοξείδιο του αζώτου είναι μια ανόργανη ένωση που έχει τον χημικό τύπο N2O5 Το ονομάζουμε πεντοξείδιο του αζώτου. Είναι ένα δυαδικό οξείδιο του αζώτου. Επιπλέον, είναι ασταθές και μπορεί να λειτουργήσει ως επικίνδυνο οξειδωτικό. Η μοριακή μάζα της ένωσης είναι 108,01 g/mol. Εμφανίζεται ένα λευκό χρώμα στερεό.
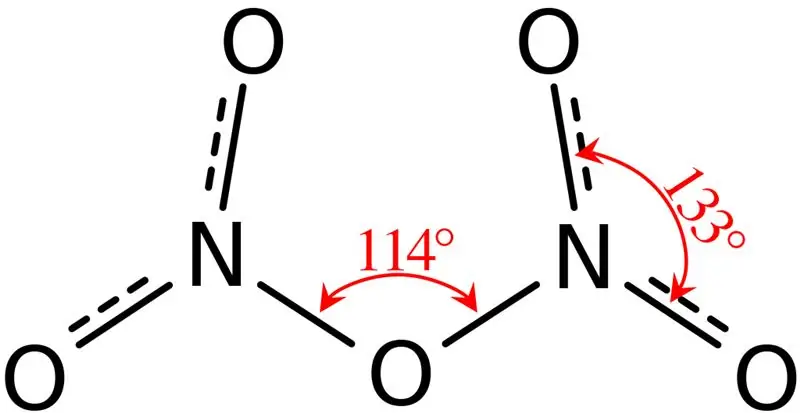
Εικόνα 02: Δομή του πεντοξειδίου του δινιτρογόνου
Επιπλέον, το σημείο τήξης αυτής της ένωσης είναι 41 °C και στους 47 °C αυτή η ένωση υφίσταται εξάχνωση. Αυτή η ένωση αντιδρά με το νερό, δίνοντας νιτρικό οξύ. Επιπλέον, το μοριακό σχήμα του μορίου του πεντοξειδίου του αζώτου είναι επίπεδο. Μπορούμε να παράγουμε αυτή την ένωση μέσω αφυδάτωσης του νιτρικού οξέος με πεντοξείδιο του φωσφόρου.
Ποια είναι η διαφορά μεταξύ του μονοξειδίου του αζώτου και του πεντοξειδίου του αζώτου;
Το μονοξείδιο του αζώτου είναι μια ανόργανη ένωση με τον χημικό τύπο ΟΧΙ ενώ το πεντοξείδιο του δινιτρογόνου είναι μια ανόργανη ένωση με τον χημικό τύπο N2O5 Η βασική διαφορά μεταξύ του μονοξειδίου του αζώτου και του πεντοξειδίου του αζώτου είναι ότι το μονοξείδιο του αζώτου είναι ένα άχρωμο αέριο ενώ το πεντοξείδιο του αζώτου είναι ένα λευκό στερεό. Επιπλέον, μπορούμε να παράγουμε μονοξείδιο του αζώτου μέσω οξείδωσης της αμμωνίας στους 850 °C παρουσία καταλύτη πλατίνας. Ωστόσο, η παραγωγή πεντοξειδίου του αζώτου γίνεται μέσω αφυδάτωσης του νιτρικού οξέος με πεντοξείδιο του φωσφόρου. Όταν εξετάζουμε το μοριακό σχήμα, το μονοξείδιο του αζώτου είναι γραμμικό ενώ το πεντοξείδιο του αζώτου είναι επίπεδο.
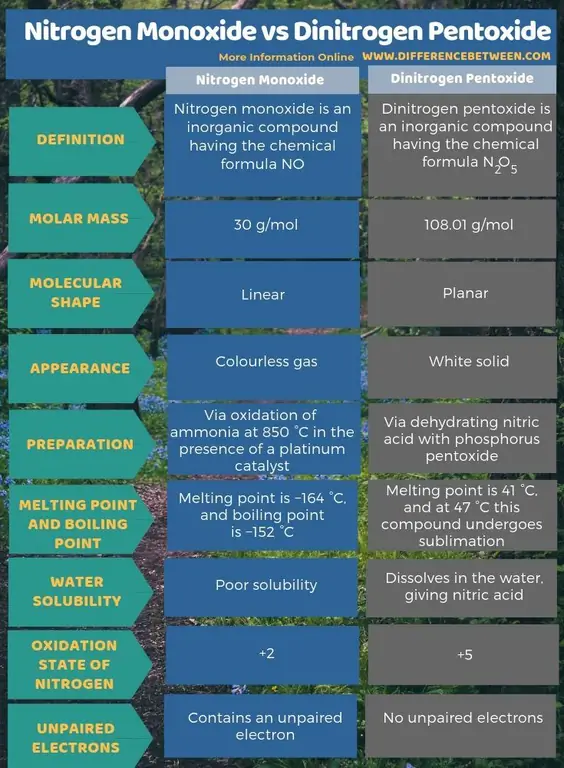
Σύνοψη - Μονοξείδιο του αζώτου έναντι Πεντοξειδίου Διαζώτου
Το μονοξείδιο του αζώτου είναι μια ανόργανη ένωση με τον χημικό τύπο ΟΧΙ ενώ το πεντοξείδιο του δινιτρογόνου είναι μια ανόργανη ένωση με τον χημικό τύπο N2O5 Η βασική διαφορά μεταξύ του μονοξειδίου του αζώτου και του πεντοξειδίου του αζώτου είναι ότι το μονοξείδιο του αζώτου είναι ένα άχρωμο αέριο ενώ το πεντοξείδιο του αζώτου είναι ένα λευκό στερεό.






