- Συγγραφέας Alex Aldridge aldridge@what-difference.com.
- Public 2023-12-17 13:36.
- Τελευταία τροποποίηση 2025-06-01 07:36.
Η βασική διαφορά μεταξύ ανθρακικού οξέος και διττανθρακικού είναι ότι το ανθρακικό οξύ είναι μια ουδέτερη χημική ένωση, ενώ το διττανθρακικό είναι μια αρνητικά φορτισμένη χημική ένωση.
Το ανθρακικό οξύ είναι ένα ασθενές οξύ που σχηματίζεται σε διάλυμα όταν το διοξείδιο του άνθρακα διαλύεται στο νερό, με χημικό τύπο H2CO3. Τα διττανθρακικά σχηματίζονται από το συνδυασμό τριών ατόμων οξυγόνου, ενός ατόμου υδρογόνου και ενός ατόμου άνθρακα με τον χημικό τύπο HCO3-.
Τι είναι το ανθρακικό οξύ;
Το Το ανθρακικό οξύ είναι H2CO3. Μερικές φορές, δίνουμε αυτό το όνομα σε διαλύματα που έχουν διοξείδιο του άνθρακα διαλυμένο σε νερό ή ανθρακούχο νερό. Αυτό συμβαίνει επειδή το ανθρακούχο νερό περιέχει μια μικρή ποσότητα H2CO3. Επιπλέον, το ανθρακικό οξύ είναι ένα ασθενές οξύ και μπορεί να σχηματίσει δύο τύπους αλάτων ως ανθρακικά και διττανθρακικά. Η μοριακή μάζα αυτής της ένωσης είναι 62,024 g/mol.
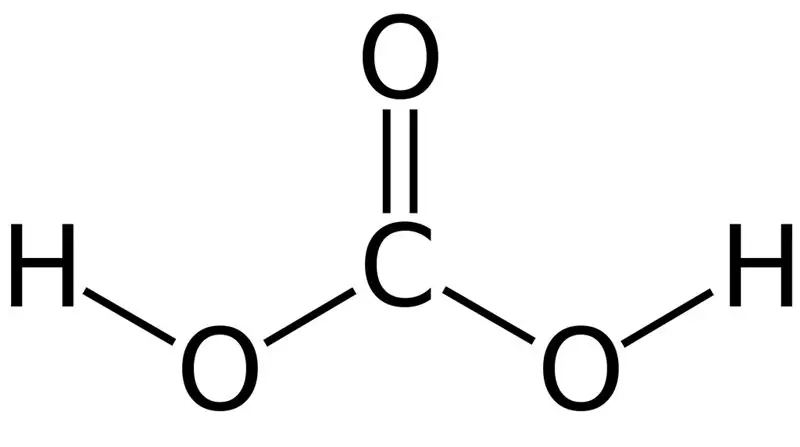
Εικόνα 01: Η χημική δομή του ανθρακικού οξέος
Όταν το διοξείδιο του άνθρακα διαλύεται στο νερό, εισέρχεται σε μια ισορροπία μεταξύ διοξειδίου του άνθρακα και ανθρακικού οξέος. Η ισορροπία έχει ως εξής:
CO2 + H2O ⟷ H2CO3
Αν προσθέσουμε περίσσεια ανθρακικού οξέος σε μια βάση, αυτό δίνει διττανθρακικό. Αλλά, εάν υπάρχει περίσσεια βάσης, τότε το ανθρακικό οξύ τείνει να δώσει ανθρακούχα άλατα. Πιο συγκεκριμένα, το ανθρακικό οξύ είναι μια ένωση καρβοξυλικού οξέος που έχει δύο υποκαταστάτες ομάδας υδροξυλίου συνδεδεμένους στον άνθρακα καρβονυλίου. Επιπλέον, είναι ένα πολυπρωτικό οξύ, το οποίο είναι ικανό να δώσει πρωτόνια. Έχει δύο αφαιρούμενα πρωτόνια, επομένως είναι ειδικά διπρωτικό.
Τι είναι διττανθρακικό;
Το διττανθρακικό σχηματίζεται από το συνδυασμό τριών ατόμων οξυγόνου, ενός ατόμου υδρογόνου και ενός ατόμου άνθρακα. Το προϊόν αυτού του συνδυασμού μπορεί να είναι ένα ιόν ή μια ένωση με περισσότερα ηλεκτρόνια από πρωτόνια. Μπορούμε να το περιγράψουμε ως ένα χημικό είδος που έχει τον χημικό τύπο HCO3-.
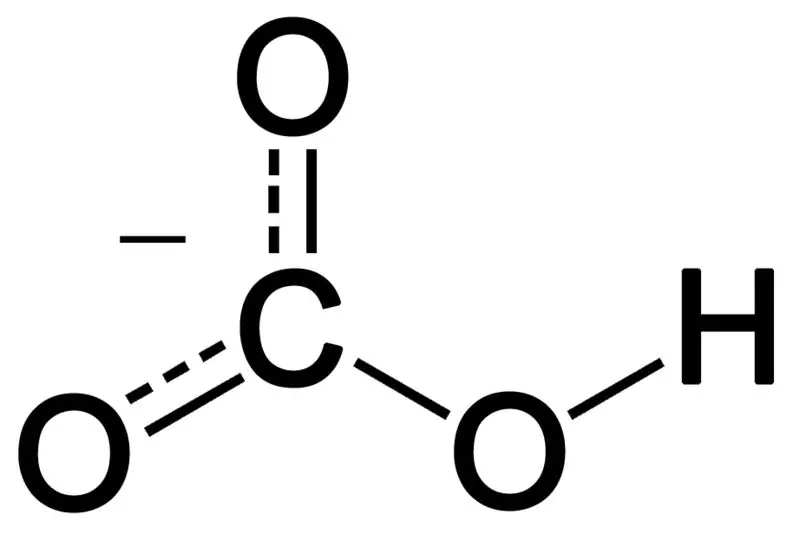
Εικόνα 02: Η χημική δομή του διττανθρακικού ανιόντος
Αυτή η ένωση είναι ένα κρίσιμο μέρος του συστήματος ρύθμισης του pH του σώματος, με απλούς όρους: είναι υπεύθυνη για τη διατήρηση του αίματος σε μια κατάσταση που δεν είναι πολύ όξινη ή πολύ βασική. Επιπλέον, χρησιμεύει ως ένας τρόπος για να διατηρείτε υπό έλεγχο τους πεπτικούς υγρούς μόλις το στομάχι ολοκληρώσει την πέψη της τροφής. Επιπλέον, το ανθρακικό οξύ στο νερό της βροχής σχηματίζει διττανθρακικά ιόντα όταν προσκρούει σε βράχους. Αυτή η ροή διττανθρακικών ιόντων είναι σημαντική για τη διατήρηση του κύκλου του άνθρακα.
Ποια είναι η διαφορά μεταξύ ανθρακικού οξέος και διττανθρακικών;
Το ανθρακικό οξύ είναι ένα ασθενές οξύ που σχηματίζεται σε διάλυμα όταν το διοξείδιο του άνθρακα διαλύεται στο νερό και ο χημικός του τύπος είναι H2CO3. Τα διττανθρακικά σχηματίζονται από το συνδυασμό τριών ατόμων οξυγόνου, ενός ατόμου υδρογόνου και ενός ατόμου άνθρακα με τον χημικό τύπο HCO3-. Η βασική διαφορά μεταξύ του ανθρακικού οξέος και του διττανθρακικού είναι ότι το ανθρακικό οξύ είναι μια ουδέτερη χημική ένωση, ενώ το διττανθρακικό είναι μια αρνητικά φορτισμένη χημική ένωση. Επιπλέον, το ανθρακικό οξύ χρησιμοποιείται στην παρασκευή αφρωδών, ανθρακούχων ποτών, στη θεραπεία δερματίτιδας, σε στοματικό διάλυμα κ.λπ., ενώ το διττανθρακικό χρησιμοποιείται σε παρασκευάσματα τροφίμων όπως το ψήσιμο (ως διογκωτικό) και δίνει την ικανότητα να αντιστέκεται στις αλλαγές του pH.
Το παρακάτω infographic συνοψίζει τη διαφορά μεταξύ ανθρακικού οξέος και διττανθρακικού σε μορφή πίνακα για σύγκριση δίπλα-δίπλα.
Σύνοψη - Ανθρακικό οξύ έναντι Διττανθρακικών
Το Το ανθρακικό οξύ είναι H2CO3. Τα διττανθρακικά σχηματίζονται από το συνδυασμό τριών ατόμων οξυγόνου, ενός ατόμου υδρογόνου και ενός ατόμου άνθρακα, με τον χημικό τύπο HCO3-. Η βασική διαφορά μεταξύ του ανθρακικού οξέος και του διττανθρακικού είναι ότι το ανθρακικό οξύ είναι μια ουδέτερη χημική ένωση, ενώ το διττανθρακικό είναι μια αρνητικά φορτισμένη χημική ένωση.






